De faibles doses d’ITKs suffisantes pour les patients ayant atteint la réponse moléculaire majeure ? La recherche de la dose « minimale efficace »
Efficacité de faibles doses d’inhibiteurs de tyrosine kinase après l’obtention de la réponse moléculaire majeure chez les patients atteints de LMC.
Efficacy of low-dose tyrosine kinase inhibitor therapy after achieving major molecular response in persons with chronic myeloid leukaemia.
D’après la communication orale de Qian Jiang et al. Abstract #S158, EHA 2023.
Contexte de l’étude
L’optimisation de la posologie des inhibiteurs des tyrosines kinases (ITKs) doit avoir pour objectif l’efficacité sur la LMC et en même temps épargner les effets secondaires. Pour autant, l’impact de faibles doses d’ITKs sur la survie après l’obtention de la réponse moléculaire majeure (RMM) n’a jamais été précisément étudié.
Objectifs de l’étude
Deux groupes de patients sont étudiés :
ceux à qui on laisse des ITKs à pleine dose et ceux pour qui on diminue de moitié la posologie d’ITK après l’obtention de la RMM. La comparaison porte, entre ces 2 groupes, sur l’obtention d’une réponse moléculaire plus profonde et le maintien de la réponse moléculaire préalable. Les ITKs étudiés sont l’imatinib, le nilotinib et le dasatinib. Le schéma de l’étude est présenté sur la figure 1. Les facteurs associés à la perte de la RMM (BCR::ABL1 > 0.1%) ou perte de la RM4 (BCR::ABL1 > 0.01%) après réduction de dose sont aussi étudiés.
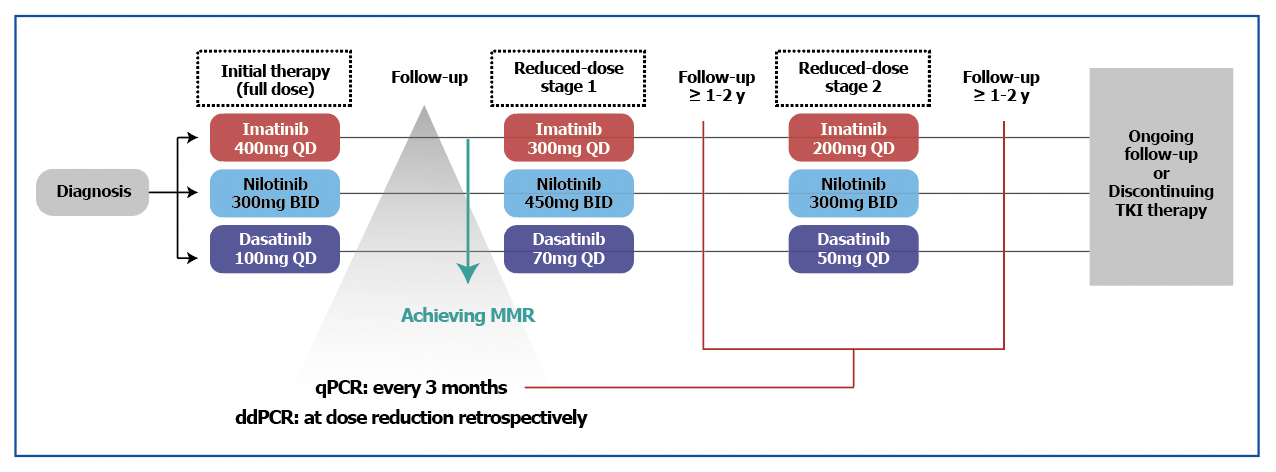
Figure 1 : schéma de réduction de la posologie d’ITK dès obtention de la RMM.
Résultats de l’étude
Sur 837 patients analysés rétrospectivement, 271 sont dans le groupe « low dose » d’ITK, leur ITK ayant été abaissé en médiane de 31 mois après l’obtention de la RMM, parmi lesquels 85% sont sous imatinib, 12% sous nilotinib et 3% sous dasatinib.
L’analyse en landmark et le score de propension montrent que l’abaissement de la posologie d’ITK n’a pas d’impact sur l’incidence cumulée à 6 ans de RM4, sur la survie sans perte de RMM, sur la survie sans perte de RM4, sur la survie sans progression ni sur la survie globale en comparaison au groupe « pleine dose » ; on note néanmoins une moindre incidence d’obtention de RM4.5.
L’analyse multivariée montre que le fait d’avoir plus de 60 ans et BCR::ABL1 >0.0078% (quasi équivalent de RM4) au moment de la réduction de dose sont les 2 critères associés à la perte de RMM.
De plus, la réduction de dose permet l’amélioration significative des effets secondaires en lien avec les ITKs et notamment la fatigue, les œdèmes et les troubles digestifs (figure 2).
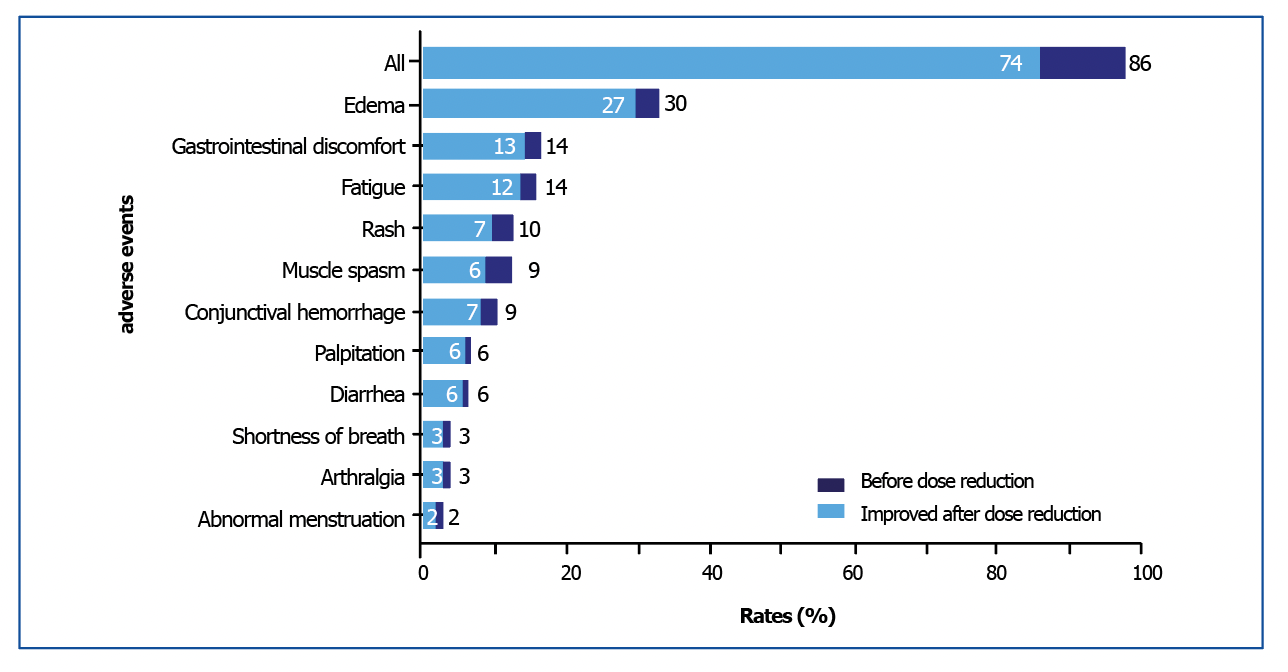
Figure 2 : réduction des effets secondaires avec la baisse de la posologie d’ITK.
Quels impacts sur les connaissances et les pratiques cliniques ?
Depuis plusieurs années maintenant, lors des consultations, on cherche à trouver la posologie « optimale », celle qui associe efficacité et tolérance, ce d’autant que bon nombre de patients ne seront pas éligibles à la TFR (= survie sans traitement). L’idée est donc de rendre le traitement le plus « supportable » physiquement et psychologiquement sur le long terme.
Grâce à cette étude, on peut conclure que la réduction de dose d’ITK est sûre dès lors que le patient a obtenu la réponse profonde (RM4). La réduction des effets secondaires est très importante et donne des arguments supplémentaires pour tendre vers cette stratégie.
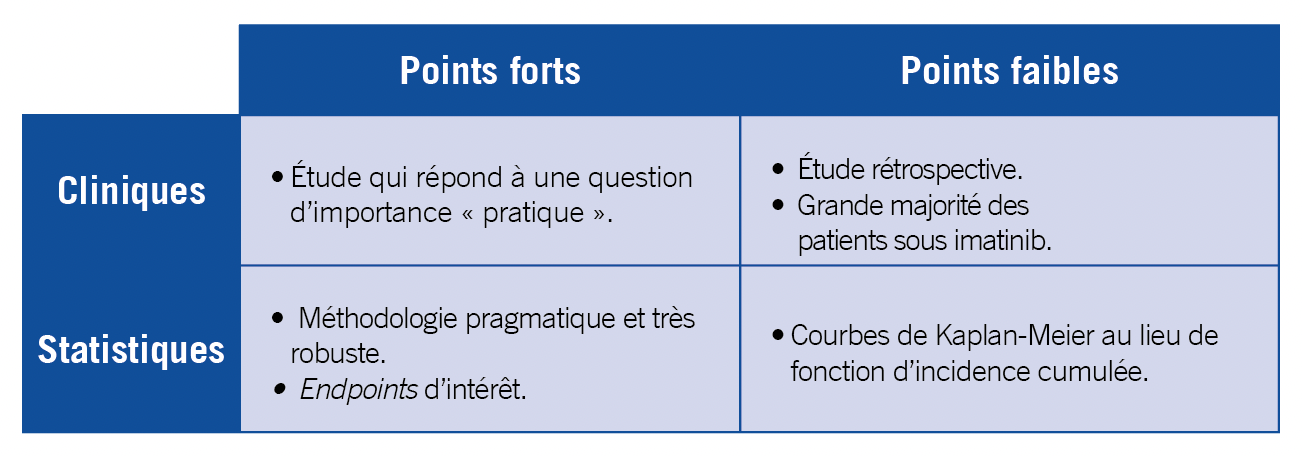
Critique méthodologique
Ce qui est présenté n’est pas un essai clinique mais une étude rétrospective, avec donc les biais inhérents à ce type de cohorte. Cette cohorte se caractérise par des patients ayant obtenu une réponse moléculaire majeure (RMM) sous dose complète (full dose) d’ITK (majoritairement de première génération avec imatinib). Sont exclus les patients ayant switché de molécule ou stoppé le traitement avant la réponse afin d’être homogène ; ce qui est un bon point. La réduction de dose pour les 3 molécules se fait en deux étapes.
Pour la méthodologie statistique, afin d’étudier le plus correctement possible l’effet de la réduction de dose, des analyses en Landmark ont été effectuées au cours du suivi depuis l’initiation du traitement. C’est plutôt bien adapté pour étudier l’aspect temps-dépendant des niveaux de dose qui sont réduits. Les endpoints analysés sont les différents niveaux de réponses moléculaires (RMM, RM4, RM4.5) et leur perte de réponse, ce sont les incontournables. Un score de propension (intégrant un nombre important de co-variables d’intérêt dont le niveau de BCR-ALB1 au temps du landmark) est utilisé pour matcher les 2 cohortes, une très bonne approche aussi pour contrecarrer les biais liés aux facteurs confondants entre groupes de patients restant en full dose versus réduction de dose. Enfin, des régressions de Cox seront utilisées pour identifier de potentiels facteurs associés à la survie sans perte de réponse (depuis l’arrêt d’ITK).
Sur 837 patients inclus, 271 ont bénéficié d’une réduction de dose. Le groupe de patients avec doses réduites était plus âgé, une proportion d’hommes un peu plus basse et plus de phases accélérées que les full dose. Ils avaient aussi un délai de RMM plus court (8 mois en valeur médiane contre 11 mois chez les full dose) et un suivi médian plus long (de 28 mois). La répartition des types d’ITKs était semblable entre les 2 groupes de même que le pourcentage de patients à bas risque. Au vu de la robustesse de la méthodologie employée, les résultats affichés dans les courbes de réponse s’interprètent directement. Il est regrettable d’avoir utilisé une courbe de Kaplan-Meier plutôt que d’une incidence cumulative afin de tenir compte des risques compétitifs (comme le décès). C’est le point faible de cette étude, cependant mineur étant donné que le nombre de décès est faible.
Dans le sous-groupe de patients avec réduction de dose, les auteurs ont directement réalisé une analyse multivariée pour détecter les facteurs liés à la perte de réponse (et ce, pour chaque niveau de réponse), plutôt que d’utiliser des algorithmes de sélection de variable. Ces modèles peuvent être encore perfectionnés, mais ce n’est pas non plus une limite pour cette étude. Les auteurs ont par la suite illustré graphiquement les résultats de ces modèles à travers des courbes de perte de réponse. Quoiqu’il en soit, voilà une étude rétrospective très bien menée !